胰腺癌:KRAS广谱靶向药,上市在即
发布日期:2025-03-25RAS(KRAS、NRAS 和 HRAS)是最常突变的癌基因之一,驱动突变主要发生在G 12(主要是 D、V、C、R 和 S)、G 13(主要是 C 和 D)和Q 61(主要是 R 和 H)上,在肺癌、结直肠癌和胰腺癌(PADC)这三种危及生命的肿瘤类型中具有显著代表性。开发泛 KRAS 抑制剂的越来越受到重视。Daraxonrasib (RMC-6236)是一款多种 RAS 突变体和野生型 (WT) 变体的非共价、有效的三重复合抑制剂,能广谱抑制所有的KRAS突变。
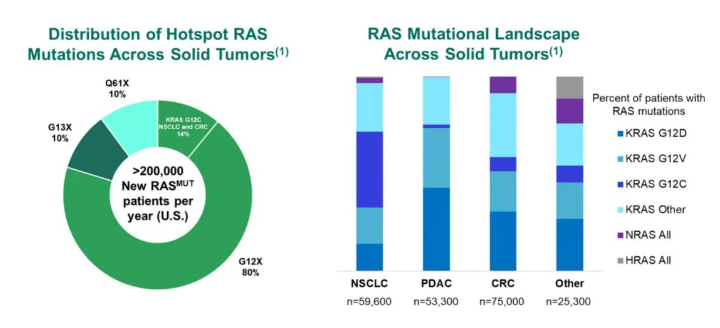
1 期研究 (NCT05379985) 共有 127 名 PDAC 患者接受了剂量范围为 160 至 300mg的药物治疗,其中 76 名接受了 300mg剂量。该队列的中位年龄为 64 岁(范围为 30-86 岁),诊断时患有 IV 期疾病(52%), 接受的抗癌治疗中位数为 2 次(范围为 1-11)。84% 的患者出现KRAS G12X 突变;其中包括KRAS G12D(32%)、KRAS G12V(32%)、其他KRAS G12X 突变(20%);16% 的患者有其他RAS突变。
2025年公布的 1 期研究 (NCT05379985) 的最新结果显示,在接受 300 mg Daraxonrasib (RMC-6236) 二线治疗的转移性 PDAC 患者中(n = 59),KRAS G12X 突变患者(n = 22)的中位无进展生存期 (PFS) 为 8.8 个月(95% CI,8.5-不可评估 [NE]),RAS突变患者(n = 37)的中位无进展生存期 (PFS) 为 8.5 个月(95% CI,5.9-NE) 。KRAS G12X 和RAS突变亚组的总缓解率 ( ORR ) 分别为 36% 和 27% ;这两个组的疾病控制率 (DCR) 分别为 91% 和 95%。
在KRAS G12X 和RAS突变患者亚组中,300 mg剂量组的中位总生存期 (OS) 为 NE(95% CI,NE-NE;95% CI,8.5-NE)。在 300 mg剂量组,KRAS G12X和RAS突变患者亚组中的 6 个月 OS 率分别为 100%(95% CI,100%-100%)和 97% (95% CI,79%-100%)。这两个亚组的中位随访期分别为 6.1 个月和 6.6 个月。
常见的与治疗相关的不良事件是皮疹,发生在 90% 以上的患者中。其他毒性包括腹泻 、恶心、呕吐和口腔炎。大多数是低级别,没有患者因毒性而需要停止治疗。正在进行的 RASolute 302 研究是一项全球随机 3 期临床试验,研究 daraxonrasib 作为二线治疗与化疗对先前接受过治疗的转移性 PDAC 患者的疗效。该研究将招募约 460 名确诊为 PDAC、在转移性环境中接受过 1 种先前治疗的患者。入组后,患者将按 1:1 的比例随机分配接受每日一次 300 mg daraxonrasib(n = 230)或标准治疗吉西他滨/白蛋白结合型紫杉醇、改良 FOLFIRINOX、NALIRIFOX 或 FOLFOX(n = 230)。Daraxonrasib 是第一种旨在直接抑制所有主要形式的致癌 RAS(ON)(PDAC 的常见驱动因素)的靶向药物。在每天300 mg的剂量下,daraxonrasib 表现出可控的安全性和令人鼓舞的总体反应率 [ORR]、PFS 和 OS, 将有望改变胰腺癌的治疗标准。
爱诺美康转诊到美国的患者中,有几位正在参加Daraxonrasib的3期临床试验,美国排名前列的几家癌症医院,试验名额已经接近满员,其他医院还有少量名额。另外据负责的美国主治医生所述,按照目前的进度,预计Daraxonrasib 将在2026年上半年批准上市。具体可咨询爱诺美康医学部。





