出国看病 FDA批准首个转移性肺癌抗PD-L1新药
发布日期:2016-10-20专注严肃医疗的出国看病服务机构爱诺美康获悉:2016-10-18,制药巨头罗氏旗下的基因泰克对外宣布,美国FDA批准其PD-L1免疫检查点抑制剂Tecentriq(药物名:atezolizumab)用于治疗前期治疗失败的非小细胞肺癌患者。
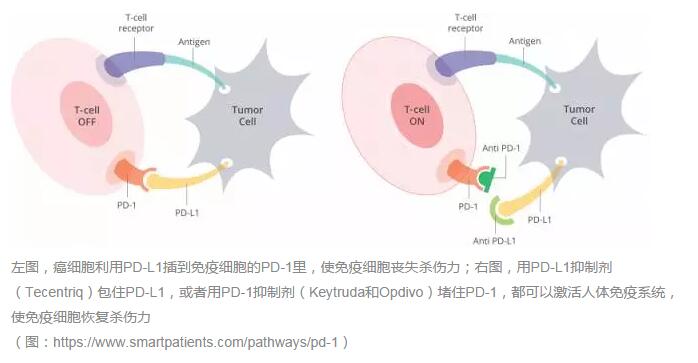
罗氏的Tecentriq将在非小细胞肺癌领域与默克的Keytruda和BMS的Opdivo这两个PD-1抑制剂正式交锋,免疫治疗正式进入“三国时代”。
Tecentriq(药物名:atezolizumab)
适应症:接受铂类药物化疗期间或之后发生进展的患者;肿瘤具有EGFR或ALK基因异常并接受相应FDA批准的靶向药物治疗后仍进展的患者。
国外批准日期:2016/10/18
中国是否获批:否
作用机制:PD-L1抑制剂
常见不良反应:疲乏、食欲下降、呼吸急促、咳嗽、恶心、便秘。
目前罗氏给Tecentriq的定价是1.25万美元,与竞争对手的价格基本持平。目前,Tecentriq的正在规划超过15项肺癌临床试验,其中包括7项一线肺癌的III期临床试验。这些研究正在评估单独使用Tecentriq或与其他药物的联合使用时的治疗效果。
出国看病服务机构爱诺美康介绍:作为第一个和唯一一个被FDA批准治疗癌症的PD-L1抑制剂,虽然Tecentriq在今年5月份被批准用于治疗膀胱癌,但肺癌显然是一个更大的市场。美国癌症协会预计,2016年美国将有超过22.4万人被诊断为肺癌,其中非小细胞肺癌将占到85%,而且其中约60%确诊的肺癌处于晚期阶段。

虽然Keytruda和Opdivo已经占得先机,但是分析人士从罗氏上周在哥本哈根欧洲医学肿瘤学会会议(ESMO)上提供的生存数据之中,看到了Tecentriq的实力与机会。
从在ESMO大会上公布的临床III期数据来看,Tecentriq将治疗失败的非小细胞肺癌患者的中位生存期提高了4.2个月。Tecentriq组的患者中位生存时间为13.8个月,多西他赛化疗组为9.6个月。Tecentriq的治疗数据「基本上是前所未有的」,基因泰克癌症免疫治疗开发主管DanChen告诉FiercePharma。 他补充说,Tecentriq的临床数据表明「Tecentriq真的有一个强大的生存效应」。
出国看病服务机构爱诺美康介绍:FDA批准的Tecentriq使用范围是很广泛的,适用于铂化疗后疾病进展的患者,或者EGFR/ALK突变阳性,但靶向治疗后仍无效的患者。与BMS的Opdivo一样,肺癌患者在接受Tecentriq治疗前不必筛查PD-L1生物标志物。但是,如果患者使用默克的Keytruda治疗,他们体内的PD-L1必须达到的特定阈值才行。这对于后入肺癌市场的Tecentriq而言,无疑是个好消息。
Tecentriq是一个全新的选择,可以帮助那些先前接受了治疗却无效的转移性肺癌患者,该药物不依赖PD-L1表达程度,比化疗更能延长生存时间。基因泰克公司CMO兼产品开发主管Sandra Horning博士告诉BusinessWire,Tecentriq是第一个,也是唯一一个被批准的PD-L1免疫检查点抑制剂。
Opdivo
在过去的15年中,晚期肺癌的生存率持续改善。肺癌幸存者肺癌基金会(ALCF)创始人Bonnie J. Addario告诉Business Wire,「Tecentriq的获批对肺癌患者而言,是有一个重大的利好,增加了肺癌患者的可用药物数量。」
Evaluate Pharma预计,到2022年Tecentriq将成为世界第14大畅销药物,预计当年的销售额会达到53亿美元。Bernstein则预计2021年Tecentriq的销售额可以达到49亿美元,Opdivo的销售额可以达到81亿美元,Keytruda的销售额则为65亿美元。如果那时阿斯利康的PD-L1抑制剂也获批的话,销售额也可以达到18亿美元。
Keytruda
出国看病服务机构爱诺美康介绍:然而,同样在今年的ESMO大会上,默克的也公布了Keytruda的多中心随机临床试验KEYNOTE-024的研究结果,Keytruda一线治疗PD-L1 高表达(至少50%的肿瘤细胞表达)的晚期非小细胞肺癌(约占所有非小细胞肺癌患者的27%-30%)的疗效明显优于化疗,与化疗相比,Keytruda显著改善临床无进展生存的主要终点(10.3个月vs 6.0个月),且不良反应较轻,该研究结果同步刊登在临床研究知名期刊《新英格兰医学》(1)上。一直以来,由于副作用大、特异性强等原因,免疫治疗都是用来挽救无药可治的癌症患者的。此次默克Keytruda的一线临床试验结果表明,免疫治疗的一线治疗效果要优于标准化疗手段,且副作用要小,是免疫治疗领域的一个重大里程碑事件。难怪一些知名学者在看到KEYNOTE-024的数据之后也惊呼,「变天了」,「地震了」。
出国看病服务机构爱诺美康认为:如此种种表明,Keytruda极有可能成为非小细胞肺癌的一线治疗方案之一。一旦默克的Keytruda被FDA批准用于非小细胞肺癌的一线治疗,Keytruda与罗氏的Tecentriq和BMS的Opdivo谁能成为大的赢家也未可知。
出国看病服务机构爱诺美康总结提到:2013年年末,肿瘤免疫治疗被《科学》杂志评选为年度十大科学突破之首;2015年免疫治疗的开创者之一James P. Allison获得拉斯克医学奖;2015年,液体活检被评选为「十大突破技术」。可以说就在近的5年之内,癌症的检测和治疗已经发生了翻天覆地的变化。就目前爱诺美康转诊的肿瘤患者而言,其中肺癌约占10%,约55%的肺癌患者获得了缓解,其中有的治疗方案正式免疫药物,相信Tecentriq的上市会为出国看病患者带来更多的选择和希望。
关键词:出国看病,爱诺美康





